秘鲁药品注册(六)更改注册
浏览1778+
根据Degimid的规定,注册完成后如果药修改注册,根据修改对人造成的健康风险的等级可以分为两类,重要修改cambios de importancia mayor, 不重要的修改cambio de importancia menor,主要是关注质量、有效性和安全性方面。
不重要的修改Cambios de Importancia Menor
更改对产品的影响很小、不影响药物质量、安全性和有效性。
a) 需要提交联系表格 “Formato de comunicaciones en el registro sanitario de productos farmacéuticos”
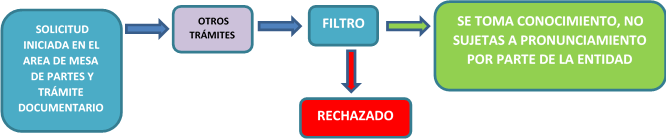
流程如下,提交后由各部门审核。文件部门审核—-其他部门审核—审查– 即通过/不通过
重要修改Cambio de Importancia Mayor
修改将显著改变药品的质量、有效性和安全性。需通过VUCE系统进行。流程也比较复杂。如下图
其他更改
- 修改药物名Cambio de nombre de producto farmacéutico – PROCEDIMIENTO TUPA 111 (Requisitos según TUPA: ftp://ftp2.minsa.gob.pe/normaslegales/tupa/RM_041-2018-MINSA.pdf, y considerar el D.S. Nº 016-2011-SA y sus modificatorias).
- 药品的转让Transferencia de registro sanitario de productos farmacéuticos, por clasificación, fabricante y país – PROCEDIMIENTO TUPA 112 (Requisitos según TUPA: ftp://ftp2.minsa.gob.pe/normaslegales/tupa/RM_041-2018-MINSA.pdf y considerar el D.S. Nº 016-2011-SA y sus modificatorias).
- 清理药品库存Agotamiento de stock de Productos Farmacéuticos – PROCEDIMIENTO TUPA 113 (Requisitos según TUPA: ftp://ftp2.minsa.gob.pe/normaslegales/tupa/RM_041-2018-MINSA.pdf y considerar el D.S. Nº 016-2011-SA y sus modificatorias).
- 药品注册证Certificado de Registro Sanitario para productos farmacéuticos – PROCEDIMIENTO TUPA 119 (Requisitos según TUPA: ftp://ftp2.minsa.gob.pe/normaslegales/tupa/RM_041-2018-MINSA.pdf y considerar el D.S. Nº 016-2011-SA y sus modificatorias).
- 药品的自由销售证明Certificado de Libre Comercialización- PROCEDIMIENTO TUPA 120 (Requisitos según TUPA: ftp://ftp2.minsa.gob.pe/normaslegales/tupa/RM_041-2018-MINSA.pdf y considerar el D.S. Nº 016-2011-SA y sus modificatorias).
- 药品出口证明Certificado de Exportación – PROCEDIMIENTO TUPA 121 (Requisitos según TUPA: ftp://ftp2.minsa.gob.pe/normaslegales/tupa/RM_041-2018-MINSA.pdf y considerar el D.S. Nº 016-2011-SA y sus modificatorias).

